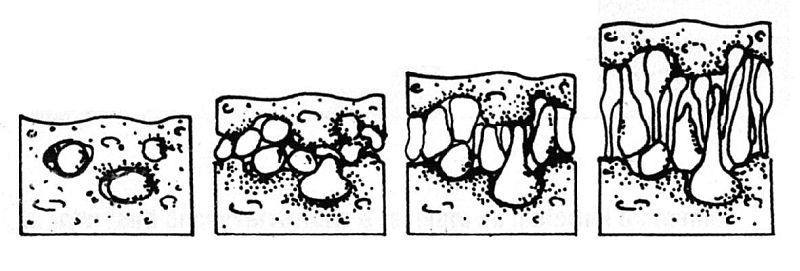
La risalita capillare e fenomeni di cristallizzazione salina
Come sappiamo l’acqua è un solvente polare per eccellenza, è una tipica molecola dipolare (per effetto della maggiore elettronegatività dell’ossigeno rispetto all’idrogeno, che produce due poli di carica). Per questa ragione le varie molecole di H2O non si dispongono in modo casuale, ma si orientano, tenute unite da forze di associazione intermolecolari, i legami a idrogeno, che si instaurano tra i poli opposti di carica. Questa struttura dipolare è la caratteristica che la rende ionizzante inoltre, il fatto che anche il valore della costante dielettrica sia elevato, le conferisce anche la capacità dissociante. Al contatto con l’H2O sostanze già di per se ioniche, come i sali, si possono dissociare e vanno in soluzione come ioni liberi idratati. L’H2O può essere trattenuta dai solidi in vario modo, la prima distinzione che possiamo fare è l’acqua essenziale, ad es. l’acqua di cristallizzazione nel gesso CaSO4 2H2O in cui le molecole di H2O fanno parte integrante della struttura cristallina del composto e sono presenti in quantità stechiometriche; e l’acqua non essenziale, la quale non è legata chimicamente al composto, ad es. l’acqua di assorbimento (ovvero la quantità d’acqua trattenuta dalla superficie di un solido), l’acqua di absorbimento (rappresenta una fase condensata trattenuta dagli interstizi o capillari dei solidi colloidali o gels), l’acqua di occlusione (è quella intrappolata nelle cavità microscopiche dei solidi cristallini), infine l’H2O può essere dispersa in un solido sotto forma di una soluzione solida.
Tutti i processi di deterioramento dipendono dall’instabilità del sistema aria-acqua-manufatto, cioè dalla quantità e dalla velocità con cui i materiali scambiano l’acqua con l’ambiente, in base alle loro specifiche caratteristiche di porosità e igroscopicità.
La temperatura sia dell’aria che dell’acqua varia costantemente nel corso della giornata e ancor di più nell’arco di un anno. La quantità di vapore d’H2O presente nell’aria varia a sua volta non solo in conseguenza ai cambiamenti di temperatura e dei relativi fenomeni di condensazione, ma soprattutto in rapporto alle vicende meteorologiche locali, con scambi continui di aria più o meno umida e calda dall’esterno all’interno dell’ambiente e viceversa.
Umidità meteorica
Il vapore acqueo che si forma sulla superficie della Terra si immette continuamente nell’atmosfera e, a seconda della temperatura l’aria, può assorbire una data quantità di vapore. Il contenuto massimo di umidità ad una determinata temperatura viene definita concentrazione di saturazione a cui corrisponde una pressione di vapore massima detta pressione di saturazione (ps).
Un parametro caratteristico dell’umidità meteorica è il grado igrometrico, ovvero il rapporto tra la concentrazione reale di H2O nell’aria e la concentrazione necessaria alla saturazione ad una certa temperatura. Più l’aria è fredda più basso sarà il suo contenuto d’acqua, invece se si raffredda dell’aria calda e umida si raggiungerà una temperatura in cui l’aria sarà satura di H2O; abbassando ulteriormente la temperatura, parte del vapore acqueo si trasformerà in liquido. Questa temperatura viene definita come temperatura di rugiada o temperatura di condensazione. La massa di vapore acqueo presente nell’unità di volume di aria umida è l’umidità assoluta UA. L’umidità molare UM, invece, è il numero di moli di vapore acqueo che occupa una mole di aria secca. A sua volta il rapporto, moltiplicato 100, tra l’umidità molare dell’aria e l’umidità molare satura di vapore nelle stesse condizioni di pressione totale e temperatura, viene definito umidità percentuale (UP).
L’umidità relativa percentuale, detta umidità relativa (UR) rappresenta il rapporto, moltiplicato 100, tra UA dell’aria e l’UA dell’aria satura di vapore nelle stesse condizioni di pressione totale e temperatura.
Umidità di condensazione
L’aria può contenere, ad una certa temperatura, una quantità massima di vapore acqueo che rappresenta il 100% di UR, se la concentrazione di umidità va oltre questo valore l’acqua tenderà a condensare su superfici fredde o a restare nell’aria in condizioni di sopra-saturazione sotto forma di nebbia. La condensazione può verificarsi sia a causa di un generale abbassamento di temperatura, sia in seguito a migrazioni del vapore acqueo in zone a temperatura più bassa. In base alla struttura dei materiali, la condensazione può presentarsi sotto forma di goccioline, se si tratta di superfici impermeabili come la ceramica, o sotto forma di macchie scure generate dallo sviluppo di muffe, funghi e batteri se l’umidità viene assorbita dalla porosità del materiale come nel caso di intonaci, laterizi, pietre porose, gesso, etc.
L’umidità può essere acquisita dai materiali, oltre che per assorbimento e absorbimento, anche per condensazione capillare nei pori estremamente fini con formazione di un menisco. La condensazione capillare deriva dal fatto che la pressione di vapore (p”) al di sopra di un menisco curvo è differente dalla pressione di vapore di una superficie d’acqua piatta (p’). In particolare se la curvatura del menisco è negativa quindi p”>p’ si ha la condensazione capillare, caso dei materiali idrofili. Se la curvatura è positiva p”<p’ non si ha condensazione, caso dei materiali idrorepellenti. Più i capillari sono sottili, più il menisco sarà curvo e più bassa sarà la pressione di vapore all’interno del capillare; se la pressione di vapore dell’aria è più alta di quella del capillare, una parte del vapore acqueo dell’aria si condenserà nel menisco.
L’umidità di condensazione superficiale si manifesta su pareti murarie fredde caratterizzate da temperature inferiori alla temperatura di rugiada, quando vengono a contatto con aria calda e umida.
I movimenti dell’Acqua
La risalita capillare
Il contatto delle fondazioni con l’acqua in un il terreno fortemente umido o addirittura con una falda freatica, provoca la risalita verticale dell’H2O all’interno del manufatto per effetto dell’assorbimento capillare. L’altezza di risalita capillare è inversamente proporzionale al diametro dei pori dei materiali, ad esempio in muri di mattoni la cui porosità varia tra 1 e 10 micron, l’altezza massima teorica di risalita varierà tra 15 cm e 1,5 m.
La bassa igroscopicità dei mattoni fa supporre che i valori massimi teorici dell’altezza della risalita debbano essere più elevati in murature costituite da materiali più igroscopici (com’è il caso di tutte le malte e della maggior parte delle pietre da costruzione). Nella realtà è difficile che ci si possa mai trovare di fronte a murature in cui l’altezza massima dell’umidità abbia raggiunto valori vicini a quelli teorici, perché in una muratura reale l’altezza effettivamente raggiungibile dall’umidità è sempre inferiore a quella massima potenziale; cioè l’altezza che l’acqua raggiungerebbe se si impedisse l’evaporazione delle sottostanti superfici della stessa muratura. Tale evaporazione fa in modo che, a mano a mano che cresce il livello della risalita, diminuisce il contenuto dell’umidità della muratura, fino a una soglia in cui se non si verifica più crescita, non lo si deve a scarsità d’acqua alla base del muro, ma alla prevalenza dell’evaporazione sull’assorbimento capillare.
Se ci troviamo di fronte a casi di livelli alti di umidità di risalita (superiori a 2 m), ciò potrebbe dipendere da fattori che impediscono o ritardano l’evaporazione sulle superfici più basse del muro, ad es. casi di zoccolature in materiali poco porosi, arredi o suppellettili vari ammassate contro le facce di una muratura; che impediscono una normale ventilazione delle parti più basse delle superfici.
Le varie forme in cui si manifesta l’H2O di capillarità sono: macchie di umidità, distacco di intonaci, distruzione delle malte di connessione, cristallizzazione dei sali, degrado di pietre, laterizi, etc.
La Condensazione
Come abbiamo detto ad ogni temperatura corrisponde un determinato valore di massima concentrazione del vapore d’acqua nell’aria. Quando il vapore, in condizioni di massima concentrazione, viene a contatto con una superficie più fredda (cioè che abbia una temperatura pari o inferiore alla temperatura di rugiada specifica del vapore d’acqua) si ha il fenomeno della condensazione, ovvero la formazione di un velo di H2O liquida sulla superficie più fredda. Questo velo di acqua sarà più o meno rapidamente aspirato all’interno della parete per capillarità. L’umidità di condensazione può formarsi anche all’interno della parete, basta che la temperatura del materiale sia inferiore a quella di rugiada per il vapore d’acqua contenuto dalla parete stessa, questo fenomeno definito condensazione interstiziale è frequente nelle antiche murature di spessore abbastanza grande. I casi più frequenti di condensazione interstiziale si verificano nelle zone di maggiore disomogeneità delle murature. La condensazione può verificarsi anche all’interno dei pori, in presenza però di altissima umidità relativa e con pori estremamente piccoli (con un raggio inferiore a 0,5 micron).
Il formarsi di H2O di condensazione all’interno dei materiali lapidei o di murature dà solitamente luogo a una rapida migrazione dell’acqua stessa verso zone più asciutte, se però nella zona di condensazione la temperatura scende e si forma il ghiaccio: l’umidità migrerà verso il ghiaccio, perché le zone a contatto con questo risulteranno in ogni caso le più asciutte. In ambienti con alta umidità relativa, l’applicazione all’esterno della parete di materiali che costituiscano comunque barriera al vapore d’acqua, favoriscono il formarsi della condensazione interstiziale, per aumento del contenuto d’acqua della parete.
A differenza dell’umidità di risalita e di quella per infiltrazione localizzata da pioggia o da perdite da condutture, è raro per l’umidità di condensazione riuscire a localizzare con precisione la zona d’insorgenza del fenomeno. Gli effetti visibili dell’uscita (e non dell’entrata dell’umidità) di solito sono efflorescenze o aloni biancastri dai contorni indefiniti.
Molto spesso si verifica il caso in cui la condensa dipenderà anche dalla preesistenza, sulla superficie o all’interno dei materiali lapidei, di una certa quantità d’H2O che potrà dipendere da umidità di risalita o da infiltrazione. E’ difficile ricostruire il reale meccanismo dei danni da umidità, quando si vuole distinguere con esattezza l’origine, c’è un caso in cui l’umidità di condensazione è piuttosto facile da diagnosticare: quando il fenomeno interessa zone ben delimitate, sulle quali l’acqua di condensa ristagna in superficie o penetra assai poco. In questo caso si manifestano macchie scure che ripetono fedelmente la forma del corpo solido, immediatamente sottostante, ‘più freddo’ perché dotato di alta compattezza e conducibilità termica (travi di ferro o blocchi di pietra coperti da strati d’intonaco di piccolo spessore).
Anche gli angoli costituiscono zone più fredde di questo tipo, cioè ben delimitate e scarsamente assorbenti. Il danno si manifesta con macchie scure, invece che bianche, perché la polvere presente nell’atmosfera si accumula di più nelle superfici fredde che su quelle calde.
L’evaporazione
Dal punto di vista conservativo, tutti i danni da umidità insorgono non al momento in cui il materiale assorbe acqua (fatta eccezione per i danni meccanici da dilatazione o rigonfiamento e per la minore resistenza meccanica che l’umidità produce in molti materiali igroscopici), ma quando l’acqua evapora e il materiale si asciuga. Un corpo poroso che viene esposto all’aria dopo immersione in acqua per un tempo abbastanza lungo da esserne permeato, si asciuga per evaporazione fino a raggiungere un determinato contenuto di umidità igroscopica. In alcuni casi il processo di asciugatura per evaporazione può spingersi oltre la condizione di equilibrio tra contenuto d’umidità igroscopica e UR, (ad es. se un materiale viene riscaldato si asciuga di più di quanto gli consentirebbe l’umidità relativa presente nell’aria). A parte queste eccezioni, l’evaporazione dell’umidità da un materiale è sempre effetto di una diminuzione dell’UR dell’aria; considerato che nei nostri climi, l’umidità relativa difficilmente scende al disotto del 30%, nessun materiale igroscopico è mai completamente asciutto.
Ovviamente la velocità di evaporazione aumenta in presenza di una corrente d’aria, ma qualunque sia la velocità l’evaporazione rimane costate fino a quando tutta la superficie interessata dal fenomeno è uniformemente bagnata in ogni suo punto da uno stesso quantitativo d’umidità. Questa condizione di uniformità non può essere di lunga durata perché i pori piccoli esercitano una maggiore forza di attrazione e quindi l’acqua evapora prima dai pori più grandi e ancora prima da buchi, fratture, etc.
Man mano che si formano questi punti più asciutti o meno umidi, l’umidità delle zone circostanti tende a confluire verso di essi, spostandosi lateralmente e in profondità, invece che verso la superficie. Questo comporta un rallentamento della velocità d’evaporazione e uno spostamento verso l’interno del fronte di umidità.
Questa continuerà lentamente ad evaporare, con una velocità inversamente proporzionale alla distanza che la separa dalla superficie; il punto in cui si produce questo scarto nella velocità dell’evaporazione viene chiamato contenuto critico d’umidità.
Per comprendere i danni causati dal fenomeno dell’evaporazione dobbiamo esaminare l’interno del corpo poroso, più precisamente la zona in cui si è attestato il fronte dell’umidità. Abbiamo visto che a una determinata temperatura e UR, la velocità dell’evaporazione è costante, nel momento in cui il fronte dell’umidità coincide con la superficie del materiale, non appena il fronte arretra, la velocità di evaporazione diminuisce.
Per ogni materiale il contenuto di umidità igroscopica è in relazione all’umidità relativa dell’aria, cioè aumenta e diminuisce con essa.
Sali solubili
L’acqua all’interno delle murature è sempre presente sotto forma di soluzione salina da cui possono separarsi sali anidri o idrati che provocano danni ai materiali. La migrazione e ricristallizzazione dei sali solubili trasportati dall’acqua costituisce il principale meccanismo di alterazione dei materiali lapidei. La forma e l’entità del danno dipendono dalla porosità e dalla igroscopicità del materiale. L’H2O, soprattutto se molto pura, provoca lo scioglimento dei sali che incontra nel suo percorso per depositarli altrove; inoltre l’acqua proveniente dal suolo si carica dei sali che questo contiene e, proseguendo il suo cammino attraverso i materiali porosi verso la superficie d’evaporazione, li trasporta nel suo percorso. Lo stesso accade per l’H2O d’infiltrazione, nel suo viaggio inverso, dall’alto al basso.
La solubilità dei sali è molto variabile, ci sono sostanze praticamente insolubili come il cloruro d’argento e sali molto solubili come il cloruro o il solfato di sodio. Il trasferimento dei sali dipende, quindi, dalla loro solubilità e dai flussi d’acqua all’interno dei materiali porosi, flussi che a loro volta sono influenzati dalla presenza di sali che possono dar luogo a variazioni di viscosità, cambiamenti di tensioni superficiali e differenze di pressioni osmotiche.
I sali solubili, che si possono trovare nei manufatti lapidei, possono avere differenti origini:
– sono parte integrante delle murature prime;
– sono inerenti ai processi di fabbricazione dei materiali;
– derivano da reazioni e scambi con l’atmosfera che avvolge il manufatto;
– provengono dal terreno sul quale il monumento è stato costruito;
– derivano dall’azione di biodeteriogeni;
– sono generati dalla corrosione elettro-chimica dei metalli;
– si formano in seguito all’utilizzo di prodotti per la pulitura e il consolidamento della pietra, o a tecniche di restauro inappropriate o inadatte.
I sali che con più frequenza si trovano nei materiali lapidei sono:
I solfati che sono sali molto mobili, disciolti nelle acque naturali di cui rappresentano uno dei maggiori costituenti, sono anche contenuti nei leganti aerei e idraulici, nelle rocce, nelle atmosfere inquinate, nelle atmosfere marine:
– solfato di calcio, si presenta in varie forme idrate come:
gesso (CaSO4 2H2O)
bassanite (CaSO4/1/2H2O)
anidrite (CaSO4)
– solfato di magnesio, presente in varie forme idrate, lo si trova con più frequenza in ambiente rurale come:
epsomite o sale di epson (MgSO4 7H2O)
kiersite (MgSO4 H2O)
– solfato di sodio , presente in forma idrata o anidra, lo si trova maggiormente in ambiente urbano come:
mirabilite (Na2SO4 10H2O)
thenardite (Na2SO4)
Andiamo a precisare le possibili origini dei solfati:
a) sono presenti nei terreni agricoli, le acque circolanti li possono sciogliere e se queste risalgono per capillarità ad es. in una muratura vi apporteranno i solfati che contengono;
b) l’acqua di mare contiene piccole quantità di solfati, specialmente solfato di magnesio. I venti di mare trasportano, per chilometri, sospensioni di particelle di acqua marina con questi sali;
c) a volte i materiali usati per la preparazione dell’intonaco possono contenere piccole quantità di solfati come impurezze. Anche i materiali usati erroneamente per il restauro possono causare la presenza di solfati (ad es. stuccature o iniezioni di gesso);
d) possono avere origine microbiologica, esistono alcuni tipi di microrganismi capaci di metabolizzare forme ridotte di zolfo ossidandolo a solfati, accanto ad altri microrganismi che invece producono solfuri (cioè una forma ridotta di zolfo);
e) l’inquinamento atmosferico. A causa della combustione degli idrocarburi, lo zolfo in esso contenuto viene trasformato in anidride solforosa (SO2), quest’ultima reagendo con l’ossigeno forma l’anidride solforica (SO3), a sua volta questa con l’acqua forma l’acido solforico (SO3 + H2O = H2SO4) il quale attacca il carbonato di calcio trasformandolo in solfato. Queste trasformazioni possono avvenire direttamente sul materiale lapideo, oppure l’acido solforico si può formare nell’aria e può arrivare a contatto del muro reagendo con il carbonato di calcio. Un’altra possibilità è che l’acido solforico formatosi nell’aria venga neutralizzato da sostanze basiche presenti in essa come l’ammoniaca, formando solfato di ammonio, o da carbonato di calcio (presente nel pulviscolo atmosferico) dando luogo a solfato di calcio. Vi è anche la possibilità che l’anidride solforosa venga assorbita direttamente come tale e come acido solforoso sui materiali calcarei; potrebbe così aversi la formazione di solfito di calcio, che soltanto successivamente si può ossidare a solfato.
I solfati sono pericolosi perché, non solo sono solubili in H2O, ma possono esistere in strati di idratazione diversi e possono cristallizzare con diverse quantità di H2O a seconda della temperatura e dell’umidità relativa.
Ad ogni stato di idratazione corrisponde un volume specifico diverso, ogni volta che si verifica la trasformazione da uno strato all’altro si ha una variazione di volume. Quando, per l’aumento dell’UR, si ha il fenomeno dell’idratazione, il sale aumenta di volume esercitando una pressione (pressione di idratazione) sulle pareti dei capillari presenti nella struttura porosa di un materiale. Quando questa pressione supera la resistenza delle pareti queste vengono rotte, l’intera struttura diventa più porosa e quindi più suscettibile all’ulteriore azione dell’umidità e dei sali.
I carbonati di Na e K derivano dai rispettivi ossidi contenuti nei leganti idraulici che vengono carbonatati dalla CO2 dell’atmosfera. I carbonati si trovano anche nelle acque naturali e negli inerti delle malte.
– carbonato di sodio, si trova in varie forme idrate:
natron o natrite (Na2CO3 10H2O)
Il carbonato di calcio, oltre ad essere presente come elemento costituente nei marmi e nelle pietre calcaree, lo troviamo anche negli affreschi e nei dipinti murali in generale, in quanto si forma per carbonatazione (Ca(OH)2 + CO2 > CaCO3 + H2O) della calce nell’intonaco. E’ pochissimo solubile in H2O, può però essere solubilizzato come bicarbonato quando nell’acqua sia presente una quantità sufficientemente elevata di anidride carbonica. La CO2 sciogliendosi nell’H2O, presente nel muro umido, dà luogo alla formazione di acido carbonico, che reagisce con il carbonato di calcio, formando il bicarbonato che è più solubile. Si stabilisce un equilibrio tra queste diverse specie chimiche: carbonati – anidride carbonica + acqua – bicarbonato; ma man mano che il muro comincia ad asciugarsi e si verifica l’evaporazione, l’equilibrio si sposta a favore della formazione di carbonato di calcio, il quale essendo poco solubile, si deposita rapidamente sulla superficie. Abbiamo due effetti negativi:
a) si forma una patina bianca che tende a coprire la superficie,
b) l’impoverimento degli strati più interni, che perdono una parte del loro carbonato di calcio.
I nitriti e nitrati. I nitriti non si trovano molto spesso nei materiali lapidei, si ossidano rapidamente trasformandosi in nitrati. La decomposizione di materiale organico azotato produce nitriti: si possono trovare questi tipi di sali su un materiale lapideo se vi sono infiltrazioni di acque di scarico o comunque provenienti da zone in cui esiste materiale organico in via di decomposizione.
– I nitrati di calcio e magnesio cristallizzano solo quando l’UR raggiunge valori inferiori al 50% :
nitrocalcite (Ca(NO3)2 4H2O)
nitromagnesite (Mg(NO3)2 6H2O)
I nitrati possono avere la stessa origine dei nitriti oppure possono provenire dal terreno agricolo o se nelle vicinanze del manufatto lapideo esistono delle vecchie tombe. Inoltre nella combustione degli idrocarburi si producono molecole organiche diverse e ossidi di azoto, quest’ultimi attraverso una complessa serie di reazioni formano acido nitrico che, reagendo con il carbonato di calcio, da luogo alla formazione di nitrato di calcio. I nitrati sono molto solubili in H2O e la loro azione nei riguardi della struttura porosa è simile a quella dei cloruri.
I cloruri
– I cloruri di calcio e magnesio non riescono a cristallizzare in condizioni normali anche se presenti in grande quantità, a causa della loro elevata igroscopicità:
antarticite (CaCl2 6H2O)
bischofite (MgCl2 6H2O)
sylvite (KCl)
Sopratutto i cloruri di sodio e di calcio sono apportati ai manufatti principalmente dal vento di mare. In alcuni casi possono dipendere dalle impurezze dei materiali usati per la preparazione dell’intonaco, in particolare la sabbia. Inoltre, alcune attività industriali (per es. la combustione di alcuni tipi di carbon fossile) possono causare la presenza di acido cloridrico gassoso nell’atmosfera. Sono sali molto pericolosi, molto solubili e spesso deliquescenti; possono assorbire umidità dall’atmosfera e trattenerla sul materiale lapideo. Quando cristallizzano formano depositi molto porosi che sviluppano forze capillari capaci di risucchiare l’acqua. La loro presenza abbassa la temperatura di transizione degli idrati e rende quindi più facile le trasformazioni da uno stato di idratazione all’altro per i sali del gruppo dei solfati. Infine, quando sono in soluzione, hanno un’elevata mobilità e possono penetrare, alterandole, in molte strutture cristalline; questi sali contribuiscono a distruggere i materiali porosi, che rapidamente tendono a polverizzare.
Il cemento può contenere alcuni sali alcalini solubili, oltre a solfati, nitriti e nitrati, aggiunti alla formulazione di partenza per ottenere particolari caratteristiche del prodotto finale. Se il muro, nel quale si compie un intervento con cemento, è soggetto a movimenti di umidità entro la struttura capillare, può accadere che una parte dei sali solubili del cemento migrino verso l’intonaco originale. Anche la diversa porosità tra cemento e malta originale può favorire il verificarsi dei fenomeni di cristallizzazione a carico di quest’ultima, se essa è più porosa. Se l’intervento con il cemento è indispensabile e insostituibile, è opportuno utilizzare quello in cui il contenuto di alcali è inferiore allo 0,2–0,3 %.
Il degrado dovuto ai sali è provocato da fenomeni di solubilizzazione, cristallizzazione, idratazione e igroscopicità; per cui se si è in una situazione di stabilità termodinamica i danni riscontrati saranno insignificanti: esistono casi in cui non sono stati riscontrati particolari alterazioni nelle murature nonostante la presenza di sali, in quanto le condizioni di temperatura e umidità sono rimaste immutate per lunghi periodi di tempo. Al contrario i fenomeni di solubilizzazione/cristallizzazione, idratazione/disidratazione e le variazioni di igroscopicità possono provocare la distruzione del materiale.
Conclusioni:
Per risolvere velocemente e con rapidità tutti i problemi di umidità muraria e muffe negli ambienti, il prodotto più adatto, ecologico, rapido e sicuro è senza alcun dubbio IgroDry.
L’unico ed innovativo prodotto in grado di risanare in pochi giorni ogni tipo di muratura.
Vai a conoscere in esclusiva le grandi opportunità che ti offre.
Tratto dalla meravigliosa tesi di laurea della Dr. Irene Franzin per UIN (Università Internazionale dell’Arte)